近期,我校生物工程学院张梁教授团队在D-手性肌醇的高效制备方面取得重要进展,研究成果“Sustainable Bioprocess for D-Chiro-Inositol Production via Metabolic Engineering of Saccharomyces cerevisiae”正式发表于Chemical Engineering Journal (IF = 13.2)。
肌醇及其立体异构体是一类重要的生物活性物质,其中肌肉肌醇(myo-inositol, MI)是自然界中最常见的形式,而D-手性肌醇(D-chiro-inositol, DCI)是MI具有特定立体构型的异构体,主要存在于豆科植物中。研究表明,DCI是治疗胰岛素抵抗、2型糖尿病和多囊卵巢综合征的重要药物,同时还具有抗氧化、抗炎活性等。目前,已有一些生物技术策略被探索用于DCI合成,但现有方法仍面临依赖昂贵MI添加、碳通量分布低效、副产物积累等显著限制,阻碍了其规模化工业应用。
张梁教授团队通过工程改造酿酒酵母构建了从木质纤维素生物质从头合成DCI的微生物平台,首次实现了酵母中DCI的从头高效生物合成,为可持续生产肌醇衍生物及推动循环生物经济提供了可扩展的绿色工艺。为实现DCI在酿酒酵母中的高效合成,团队设计了一套分阶段代谢工程策略,主要包括四个模块:(A) 强化肌醇合成途径;(B) 重定向碳代谢流;(C) 优化转运系统;(D) 重构能量代谢体系。肌醇为DCI合成的关键前体,研究人员首先通过过表达酿酒酵母内源的肌醇-3-磷酸合酶(ScIPS)及大肠杆菌来源的肌醇单磷酸酶(EcIMP),构建了肌醇合成途径。结果表明,采用强启动子PTEF1的效果优于PGAP,所得菌株C03实现了肌醇的从头合成,产量达0.35 g/L,相比野生型实现了从无到有的突破。为解决碳代谢流向乙醇发酵竞争性分流的问题,研究采用“开源节流”策略,一方面敲除磷酸果糖激酶基因(pfk2)和6-磷酸葡萄糖脱氢酶基因(zwf1),减少竞争性碳耗用;另一方面引入来源于双歧杆菌的磷酸酮酶(Bbxfpk)和克雷伯氏菌的磷酸转乙酰酶(Ckpta),同时敲除pfk1,构建非氧化糖酵解途径(NOG)。该人工旁路有效减少了丙酮酸脱羧过程的碳损失,提高了碳原子的转化效率。改造后菌株C06肌醇产量提升至1.56 g/L,乙醇产量降至3.13 g/L,比生长速率提高50%。为防止胞外产物被重新摄取并促进分泌,研究人员进一步敲除了内源性肌醇转运蛋白基因ITR1和ITR2,同时过表达水通道蛋白Fps1和甘油促进因子GlpF。该策略使肌醇产量提升至2.32 g/L。为协调肌醇合成对NADPH的高需求与细胞生长对ATP需求之间的矛盾,研究构建了一个包含三模块的合成能量系统:敲除pgi基因,强制碳流进入磷酸戊糖途径以生成大量NADPH;利用GDH1/GDH2循环将多余NADPH转化为NADH;引入线粒体外膜NADH脱氢酶(NDE1、NDE2),将胞质NADH导入线粒体驱动氧化磷酸化生成ATP。在此基础上结合适应性实验室进化(ALE),最终获得菌株C13,摇瓶发酵肌醇产量达7.32 g/L,较初始菌株提升315%。胞内辅因子测定显示NADPH水平显著提高,有效支持了目标产物的合成。在获得肌醇高产菌株后,研究进一步引入异源肌醇2-脱氢酶(IDH)和异构酶(KII),构建DCI合成途径。通过对不同来源酶的系统筛选,确定T. maritima来源IDH与G. stearothermophilus来源KII的组合最优。最终菌株C15在摇瓶发酵条件下实现DCI产量1.42 g/L,为目前酿酒酵母异源合成DCI的最高报道水平。研究进一步尝试利用农业废弃物——烟草茎秆作为碳源。在以烟草茎秆水解液为唯一碳源的补料分批发酵中,工程菌株消耗了37.47 g/L的还原糖,最终产出 3.34 g/L 的肌醇和 0.50 g/L 的DCI。这证明了该平台利用廉价生物质原料进行高附加值生产的可行性。
张梁/郭忠鹏教授团队为论文的通讯作者,我校2022级博士生许灿为第一作者。
论文链接:https://doi.org/10.1016/j.cej.2025.171466。
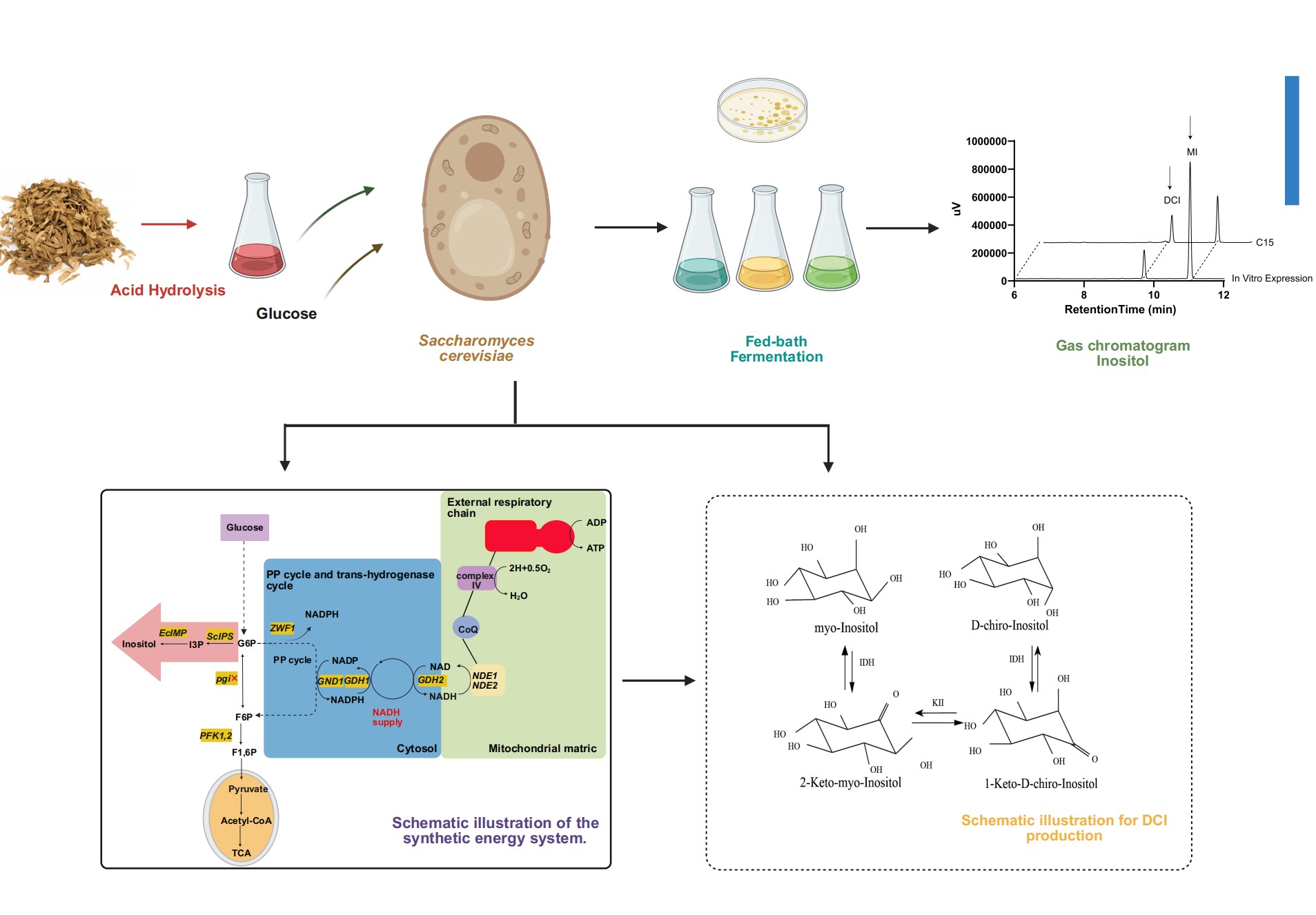
图形摘要
