近期,我校生物工程学院聂尧教授团队在羰基还原酶多性能协同改造方面取得重要进展,研究成果“Computer-Aided Directed Evolution Achieves Balanced Activity, Thermal Stability, and Selectivity in Stereoselective Carbonyl Reductase”发表于ACS Catalysis (IF = 13.1)。
在绿色化学与生物制造快速发展的背景下,酶催化因其高选择性和环境友好性,已成为手性药物及精细化学品合成的重要手段。其中,羰基还原酶能够高效催化前手性酮向手性醇转化,在多种药物关键中间体的制备中具有重要应用价值。然而,天然酶普遍存在活性不足、稳定性有限以及底物适应性较差等问题,更关键的是,多种性能之间往往相互制约:活性提升常伴随稳定性或选择性的下降,这一“功能权衡”长期制约着酶工程的发展。
针对这一核心挑战,研究团队突破传统以活性中心为主的局部设计思路,从全蛋白尺度出发构建了计算辅助进化框架。研究首先基于无监督上位性模型EVmutation,对羰基还原酶全序列进行虚拟饱和突变扫描,系统解析氨基酸残基之间的协同作用关系;在此基础上,进一步对潜在突变进行序列-结构的多维筛选。通过这一策略,原本6720个突变被大幅压缩至27个高置信候选突变。随后,研究采用贪婪组合策略逐步累积有益突变,仅通过45个突变体的实验验证,便获得了最优突变体,该突变体在模型底物2-乙酰吡啶上的催化活性达到野生型的28倍,同时在22种结构多样底物上均保持超过99%的对映选择性,并实现5.8°C的热稳定性提升。进一步的结构解析与分子动力学模拟揭示了这一多性能协同优化的内在机制。远端突变通过重塑蛋白内部的构象通讯网络,调控不同结构区域之间的动态耦合关系,从而在不破坏活性位点精细构象的前提下,提高催化活性构象的占比,并优化整体结构稳定性。换言之,该工作揭示了一种“动态协同”的分子机制,即通过全局柔性再分配,实现局部催化效率与整体稳定性的统一。本研究不仅在方法上实现了从“局部理性设计”向“全局协同进化”的转变,也在效率上大幅降低了实验筛选规模,在酶工程中具有潜在的应用前景。
聂尧教授为论文的通讯作者,我校博士后顾洁为第一作者。上述研究得到了国家自然科学基金(22378168,22508142)等项目的资助。近年来聂尧教授团队在高效氧化还原酶的创制及高附加值手性产物的绿色生产方面取得丰硕成果,相关研究成果已发表在ACS Catalysis (2022,2023,2024)、Biotechnology Advances (2022,2023,2025,2026)、Bioresource Technology (2026)等本领域权威期刊。
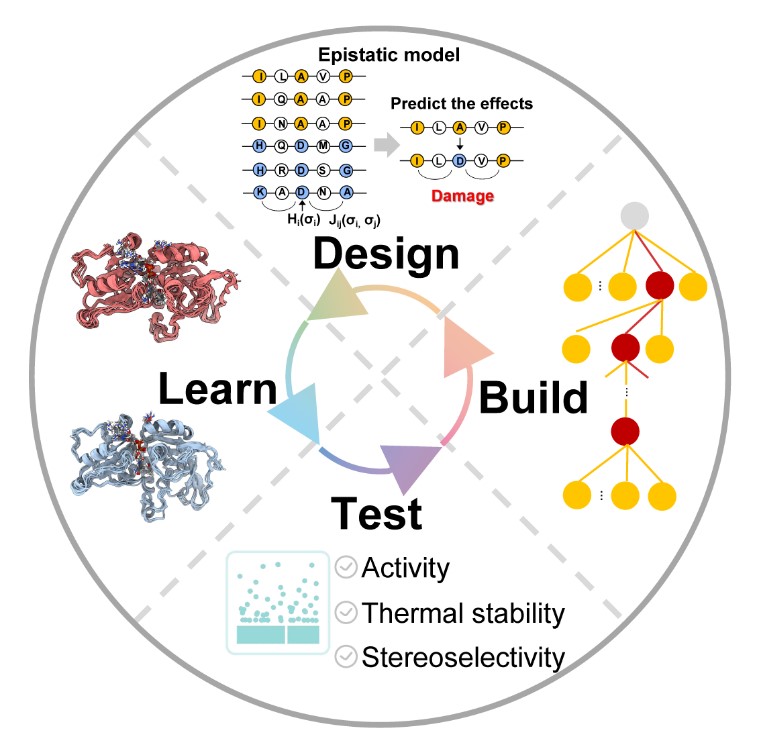
图形摘要
