近期,我校生物工程学院穆晓清教授和聂尧教授课题组在胺脱氢酶的底物特异性定向改造和高附加值手性氮杂环胺酶促催化合成方面取得重要进展,研究成果“Engineering the Substrate Acceptance of L-Amine Dehydrogenase Enables the Collective Biocatalytic Synthesis of N-heterocyclic primary amines” 正式发表于Chemical Engineering Journal (IF = 15.1) (https://www.sciencedirect.com/science/article/abs/pii/S1385894724032224)。
含氮结构基序,包括手性氨基和氮杂烷基环是天然产物、生物活性化合物和药物活性成分中的关键组分,同时含有这两种关键结构基序的手性氮杂环胺是众多重磅药物的构建砌块和合成中间体。因此,开发绿色、可用、高效的手性氮杂环胺不对称合成的生物催化剂是当前手性胺类化合物合成领域的中心主题之一。
由于水是唯一的副产物,胺脱氢酶催化的前手性酮底物的不对称还原胺化途径在手性胺的合成中极具吸引力。原则上,胺脱氢酶催化的氮杂环酮的不对称还原胺化为手性氮杂环胺的制备提供了一种直接简便的方法。然而,目前报道的胺脱氢酶数量少,底物范围有限,尚未见基于胺脱氢酶催化不对称还原胺化制备手性氮杂环胺的案例。
在此项研究中,研究人员以N-Boc-4-乙酰哌啶作为胺脱氢酶催化的氮杂环酮模型底物,基于逆行底物设计策略从小型胺脱氢酶文库中筛选出源于西伯利亚杆菌(Exiguobacterium sibiricum)的亮氨酸胺脱氢酶(L-EsAmDH)作为目标氮杂环酮底物特异性改造出发酶。随后,研究人员采用基于使用过渡底物的底物行走策略对L-EsAmDH进行底物特异性进化,通过两轮减轻酶分子底物结合口袋空间位阻的定点突变获得的双点突变体L49G/V303A成功产生了对模型底物N-Boc-4-乙酰哌啶的底物特异性,进一步的两轮迭代位点组合突变获得的四点突变体L49G/V303A/L307A/T143A对模型底物N-Boc-4-乙酰哌啶的比催化活性较双点突变体L49G/V303A提高了116.3倍。制备规模合成表明四点突变体L49G/V303A/L307A/T143A具有显著扩展的目标氮杂环酮底物范围,可催化一系列结构多样的N-Boc、N-Bn、N-Cbz取代的氮杂环酮的不对称还原胺化制备,从而相应的手性氮杂环胺,且产物对映选择性均>99%。基于结构的计算分析为氮杂环酮底物特异性的来源和催化活性的改善提供了分子见解。
此项研究首次报道了基于酶促不对称生物催化胺化合成此类手性氮杂环胺,为此类结构多样的手性氮杂环胺的生物催化绿色合成奠定了基础,并为胺脱氢酶家族成员及具有类似底物结合口袋的氧化还原酶的底物特异性及催化活性改造提供了可参考的工程指导。
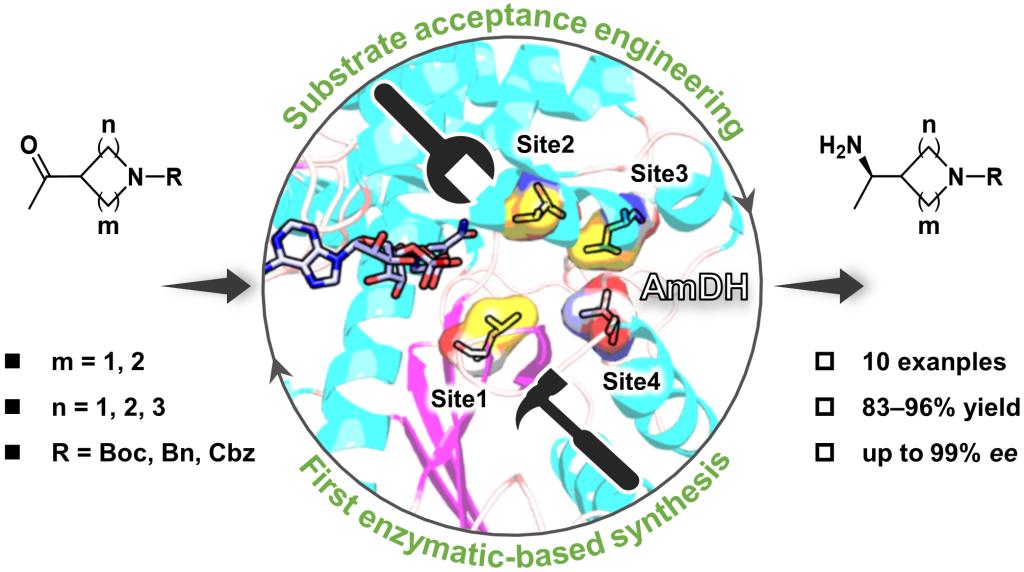
图形摘要
穆晓清教授和聂尧教授为论文的通讯作者,我校2020级博士生吴涛为第一作者。上述研究得到了国家重点研发计划(2021YFC2100100)的资助。
近年来穆晓清教授课题组在高效辅酶依赖型氧化还原酶的创制及高附加值手性产物的绿色制备方面取得丰硕成果,相关研究成果已发表在Chemical Engineering Journal(2024)、ACS Catalysis (2024,2022)、Frontiers in Bioengineering and Biotechnology (2022)、Bioresources and Bioprocessing (2022)、Metabolic Engineering (2021)、Biotechnology for Biofuels (2021)、ChemCatChem (2021)、Applied Microbiology and Biotechnology (2021)等本领域权威期刊。
