近期,我校生物工程学院周楠迪教授团队在肿瘤标志物MUC1检测方面取得重要进展,研究成果“A fluorescence and SERS dual-mode biosensor for quantification and imaging of Mucin1 in living cells”正式发表于Biosensors and Bioelectronics(IF = 10.7)(https://doi.org/10.1016/j.bios.2024.116964)
粘蛋白1(MUC1)是一种主要分布于腺上皮细胞的跨膜糖蛋白,它与肿瘤的发生、发展和转移密切相关,MUC1在90%以上的人乳腺癌中异常表达,通常被认为是一种肿瘤相关抗原,用于肿瘤的诊断和生物学治疗。MUC1的常见检测方法,包括酶联免疫吸附测定、免疫荧光、免疫印迹等,通常具有分析复杂、缺乏特异性和检测成本高的缺点。因此,开发一种同时提供MUC1定量检测和影像学分析的方法具有重要意义,可为乳腺癌的准确诊断提供全面支持。
周楠迪教授团队开发了一种基于荧光(FL)和表面增强拉曼散射(SERS)的双模式生物传感器,用于MUC1的灵敏检测和活细胞成像。FL-SERS双模生物传感器由MUC1适配体和PDDA修饰的功能化量子点(QD-PDDA-Apt)与互补DNA功能化金纳米星(AuNS-cDNA-PEG)组成。该传感器通过AuNS猝灭QD的FL信号实现了MUC1的FL模式下的定量和成像,并通过AuNS的热点效应显著增强了PDDA的SERS信号(图1)。双模生物传感器对MUC1表现出高灵敏性,在101-106 fg/mL 的宽动态范围内,FL模式下的检出限为1.19 fg/mL,SERS 模式下的检出限为1.16 fg/mL;此外,该生物传感器具有优异的选择性、良好的生物稳定性和低细胞毒性(图2)。 为了进一步研究该双模传感器在细胞中的成像能力,采用了MCF-7细胞和HepG-2细胞对该传感器的成像能力进行了评估,成像结果表明该传感器具有良好的特异性并且可以实现活细胞中MUC1的双模式成像(图3)。
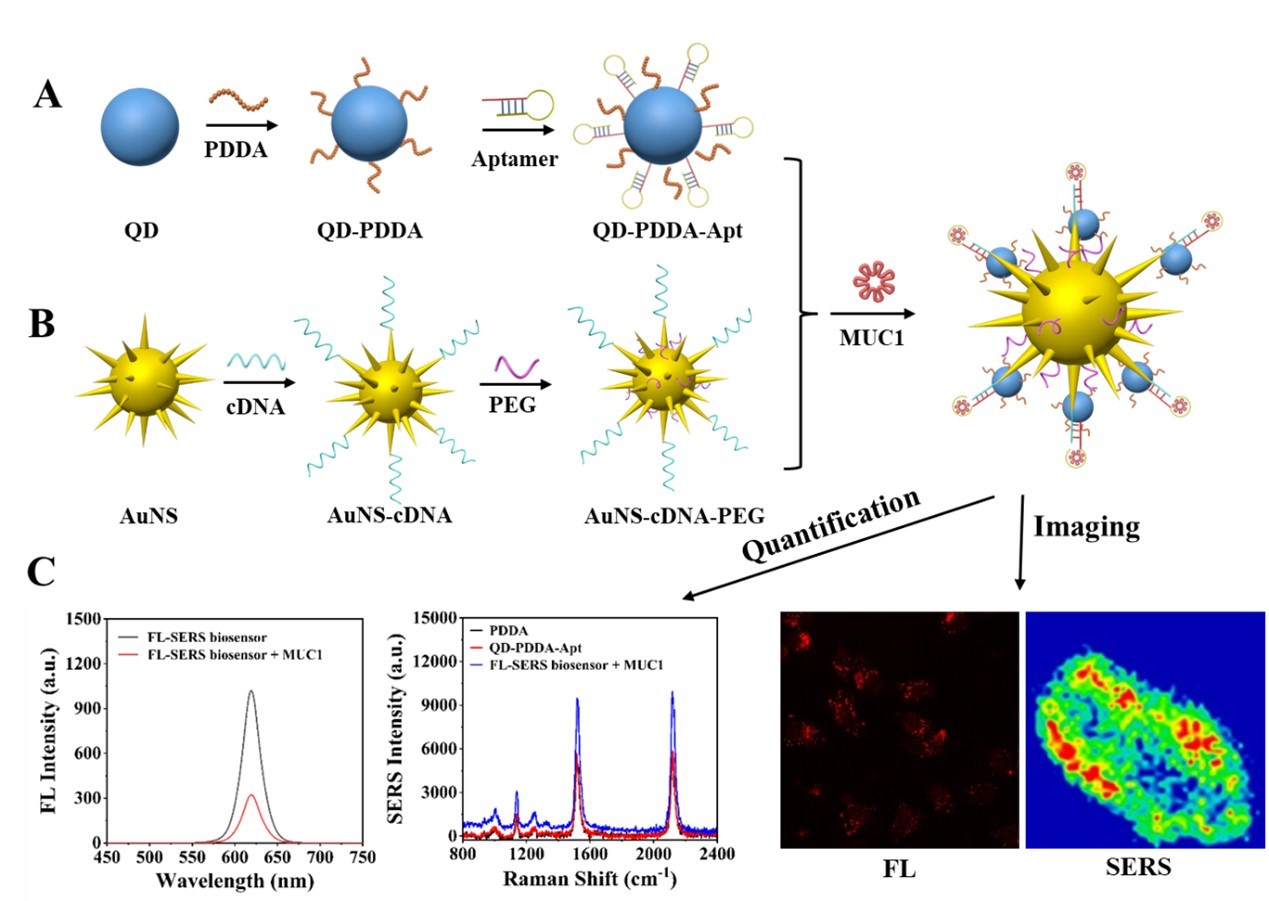
图1. 用于 MUC1 检测和成像的 FL-SERS 生物传感器示意图。(A) QD-PDDA-Apt合成;(b) AuNS-cDNA-PEG 的合成;(C) 使用构建的生物传感器对活细胞中的 MUC1 进行检测和成像。
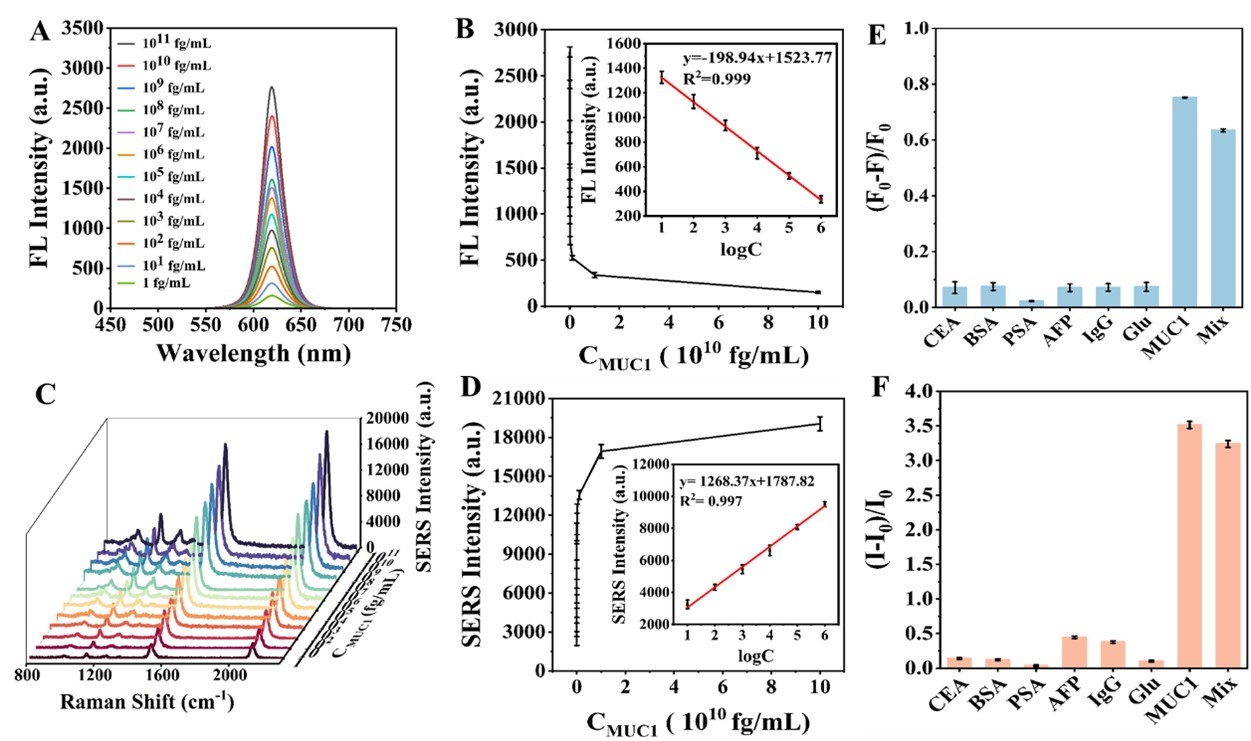
图 2.(A) MUC1 浓度梯度下 FL-SERS 生物传感器的 FL 谱图。(B) 620 nm 处 FL 强度和 MUC1 浓度的校准曲线。插图显示了 620 nm 处的 FL 强度与 MUC1 浓度的对数之间的线性关系。(C) MUC1 浓度梯度下 FL-SERS 生物传感器的 SERS 谱图;(D) 2120 cm-1 和 MUC1 浓度下的 SERS 强度校准曲线。插图显示了 2120 cm-1 处的 SERS 强度与 MUC1 浓度对数之间的线性关系; FL-SERS 生物传感器在 FL 模式 (E) 和 SERS 模式 (F) 中对 MUC1 和其他干扰物质的选择性。
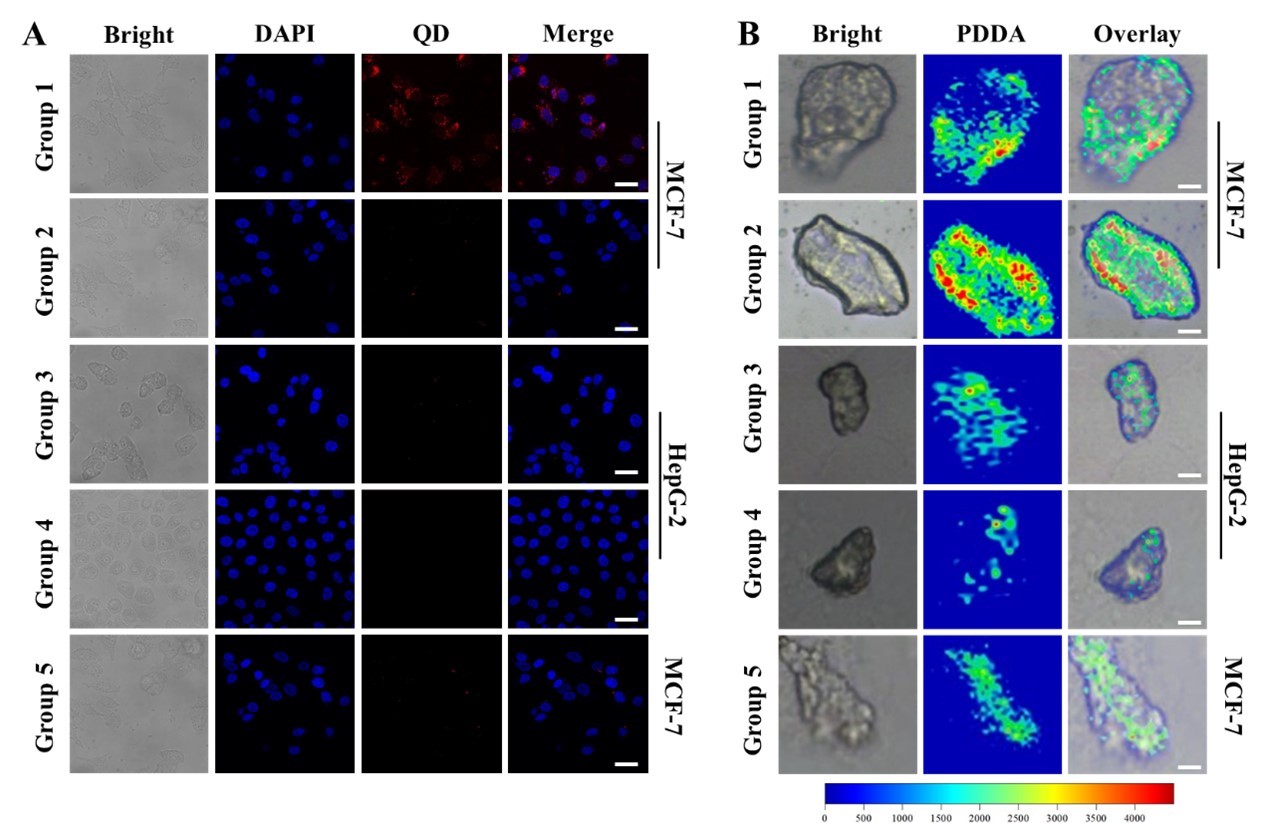
图 3.(A) 共聚焦成像和 (B) 使用 FL-SERS 生物传感器对不同细胞中的 MUC1 进行拉曼成像。第 1 组是 MCF-7 细胞的 QD-PDDA-Apt,第 2 组是 MCF-7 细胞的 QD-PDDA-Apt 和 AuNS-cDNA-PEG,第 3 组是 HepG-2 细胞的 QD-PDDA-Apt 和 AuNS-cDNA-PEG,第 5 组是 MCF-7 细胞的 MUC1 mAb、QD-PDDA-Apt 和 AuNS-cDNA-PEG。
上述研究工作中,王晓丽副教授和我校22级硕士生杨惠茹为共同第一作者,周楠迪教授和张雨婷副研究员为论文的共同通讯作者。研究工作得到了国家自然科学基金 (32371430,62301234,42177212)等资助。
近年来周楠迪教授团队研究方向包括核酸适配体的筛选优化和应用、分子诊断技术、新型纳米生物传感器的研制、智能纳米器件的构建和应用、POCT产品研制、食品安全检测、发酵过程中代谢物监测等方面。相关研究成果已发表在Chemical Engineering Journal (2024)、Aalytical Chemistry (2023)、Biosensors and Bioelectronics (2022、2022、2021)、Food Chemistry (2022)、Talanta (2022)、Sensors and Actuators B: Chemical (2021)、ACS Applied Materials & Interfaces (2021) 等本领域权威期刊。
