近日,江南大学生物工程学院、糖化学与生物技术教育部重点实验室尹健教授团队在新型糖苷类前药研究方面取得新进展,研究成果“Tandem activated caged galactoside prodrugs: advancing beyond single galactosidase dependence”发表于英国皇家化学会(RSC)旗舰期刊Chemical Science(Chem Sci 2025, 16, 7173, DOI: 10.1039/D5SC00722D),并被选为内封面文章。

图1 研究成果被选为内封面文章
β-半乳糖苷前药经肿瘤细胞(如卵巢癌等)内高表达的β-半乳糖苷酶(β-gal)激活后释放母体药物,在抗肿瘤药物领域极具应用潜力。然而,巨噬细胞、神经元细胞、衰老细胞等也存在β-gal表达升高的现象,因此,单纯依赖β-gal激活的前药有在非肿瘤组织内释放母药产生脱靶毒副作用的风险。
尹健教授团队旨在利用β-gal的高底物特异性解决β-gal肿瘤细胞分布特异性不足的问题。团队以半乳糖的羟基为修饰位点,在羟基上引入遮蔽基团,构建了全新的半乳糖苷双前药。该类双前药需首先响应遮蔽基团对应的刺激条件后裸露出半乳糖的羟基,然后才能进一步响应β-gal释放母药,被称为Tandem Activated Caged Galactoside(TACG),通过“与”门逻辑关系提升了药物释放的可控性(图2)。
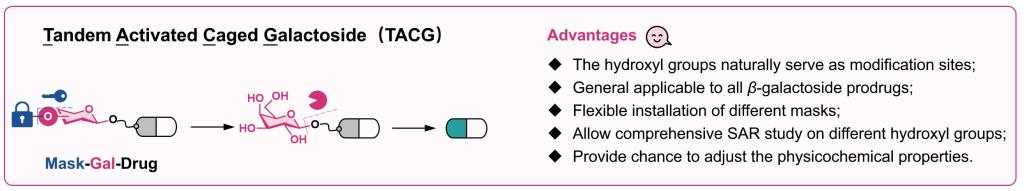
图2 串联激活的半乳糖苷双前药的设计
作者首先以半乳糖的6位羟基为修饰位点,以香豆素为报告分子,构建了一系列O6修饰的香豆素半乳糖苷。响应实验证明,这些O6修饰的半乳糖苷不被β-gal水解,只有经光照、氧化还原、生物正交等刺激条件激活裸露出6位羟基后才能进一步响应β-gal。以上结果初步证明了TACG策略的有效性。
光照激活由于其优异的时空可控性在前药领域有着广泛应用。作者接下来选择用光笼基团DMNB修饰半乳糖6位羟基,选择微管蛋白聚集抑制剂combretastatin A4(CA4)和金属离子螯合剂羟基喹啉(HQ)为药物分子,构建了双前药6-DMNB-Gal-CA4和6-DMNB-Gal-HQ。生物活性评价证实,双前药依次响应紫外光照(UV)和β-gal后释放出对应的母药并发挥抗肿瘤活性(图3)。
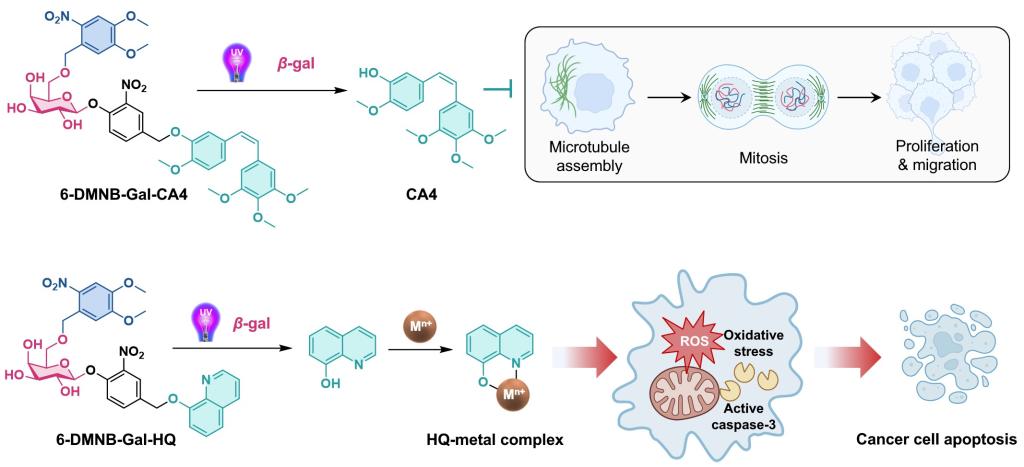
图3 双前药6-DMNB-Gal-CA4和6-DMNB-Gal-HQ依次响应UV和β-gal发挥抗肿瘤活性
接下来,作者将修饰位点从6位羟基扩展到半乳糖的2、3、4位羟基,基于糖化学正交保护策略,构建了O2、O3、O4和O6光笼集团修饰的半乳糖苷前药的合成通法(图4),并对不同羟基修饰的半乳糖苷前药的位置异构体开展了系统的构效关系研究。结果提示,O2和O6修饰的半乳糖苷的UV/β-gal双重依赖性显著高于O3和O4修饰的异构体。作者最后选择双前药2-DMNB-Gal-CA4和6-DMNB-Gal-CA4进行重点比较。细胞实验和斑马鱼实验证明,与6-DMNB-Gal-CA4相比,双前药2-DMNB-Gal-CA4经UV/β-gal双重响应展现出更优异的抗肿瘤活性。
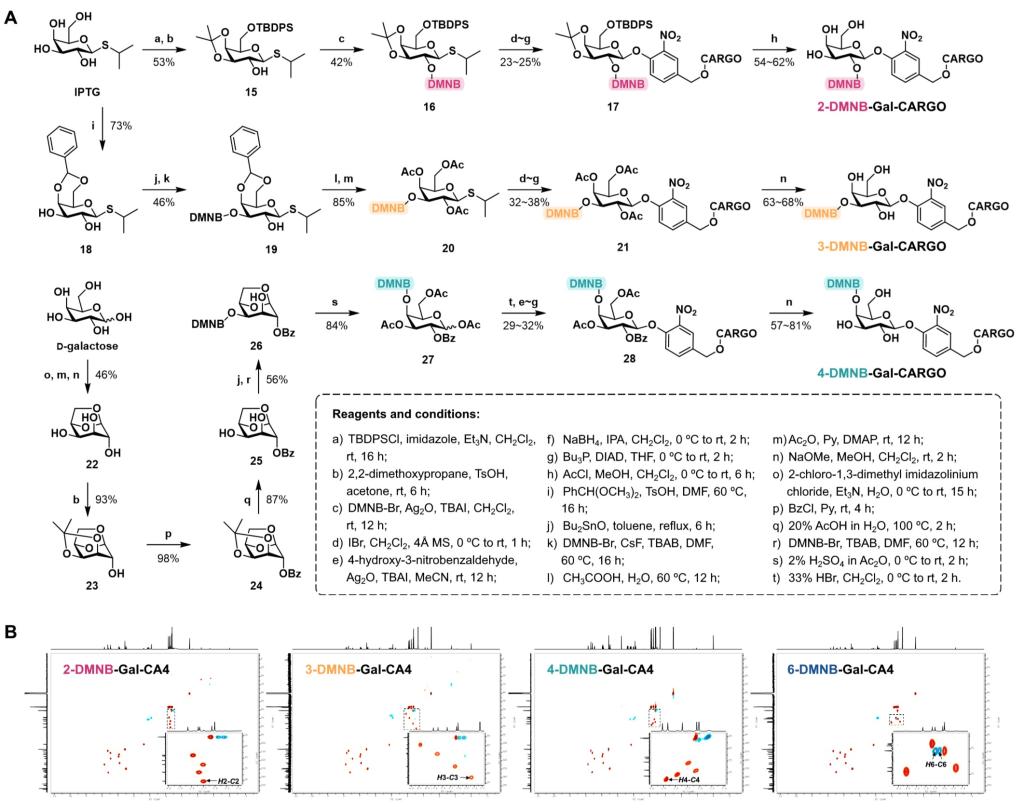
图4 半乳糖O2、O3、O4和O6光笼基团修饰的半乳糖苷前药的合成通法
本研究综合利用糖化学和糖生物学技术,创新性地利用半乳糖的羟基构建双前药,为发展药物释放可控性更高、安全性更好的半乳糖苷前药提供了新思路。TACG的设计思想可进一步扩展至葡萄糖苷前药、葡萄糖醛酸苷前药、N-乙酰氨基葡萄糖苷前药等,有望为糖苷前药的设计提供一种普适的方法,推动糖类药物的开发。
尹健教授和傅俊杰副教授为该论文的共同通讯作者,我校2020级博士研究生谭云鹰为论文第一作者。研究得到了国家自然科学基金(22325803, 22277042, 22077052)和国家留学基金管理委员会(CSC)等的资助。
