近日,我校生物工程学院饶志明教授团队在解析噬菌体防御系统作用机制方面取得重要进展,研究成果“The two-component nuclease-active KELShedu system confers broad antiphage activity via abortive infection”正式发表于Science Advances(IF=12.5)。
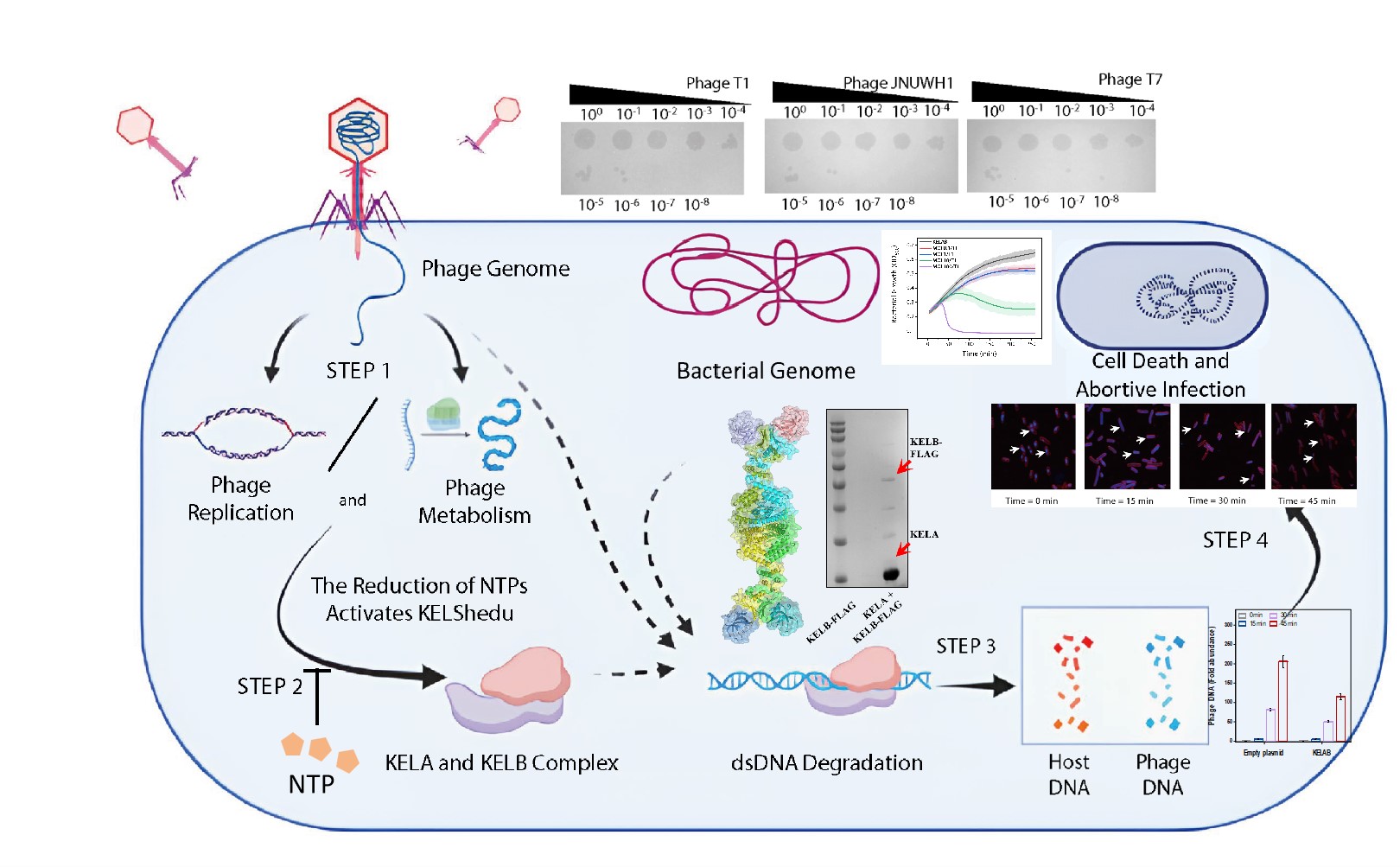
KELShedu 噬菌体防御系统抵御噬菌体侵染示意图
噬菌体是感染细菌的病毒,严重威胁有机酸、氨基酸等依赖细菌发酵的高价值工业品的工业生产。在自然环境中,噬菌体与其宿主细菌与之持续进行进化军备竞赛,推动了复杂防御和反防御机制的演化。该研究鉴定并表征了一个位于大肠杆菌中的新型双组分噬菌体防御系统——KELShedu。该系统通过“流产感染”(Abortive Infection, Abi)机制赋予宿主细菌广谱的噬菌体抗性,其由KELA(一个双链DNA结合蛋白)和KELB(一个含有DUF4263结构域的金属离子依赖性核酸酶)组成。KELA能够非特异性地结合dsDNA,而KELB则发挥依赖锰离子的核酸酶活性,能够切割多种形式的DNA,KELA和KELB通过形成复合物共同发挥抗噬菌体作用。进一步分析发现,该系统的核心激活机制依赖于细胞内NTPs(核苷三磷酸)的水平:生理浓度的NTP会抑制KELShedu系统的DNA切割活性,而噬菌体入侵导致的NTP耗竭则会激活该系统。一旦被激活,KELShedu会非特异性地降解包括宿主基因组和噬菌体DNA在内的所有细胞DNA,最终诱导细胞死亡,实现“流产感染”。阐明KELShedu系统抵抗噬菌体侵染的分子机制,不仅有助于深化对细菌防御策略的认知,也将为发掘和解析新型抗噬菌体元件提供关键理论支撑。在此基础上,进一步指导构建具有高抗性与广谱性的抗噬菌体底盘细胞,从而为以大肠杆菌为底盘细胞的高效合成氨基酸、有机酸等高价值产品的生物制造产业奠定坚实基础。
生物工程学院发酵工程专业2021级博士生张恒维和尤甲甲助理研究员为论文第一作者,张显教授、饶志明教授为论文通讯作者。研究工作得到了国家自然科学基金(32071470)、江苏省前沿技术研发计划项目(BF2024012)、江苏省研究生科研与实践创新计划(KYCX23_2501)资助。
近年来,饶志明教授团队在氨基酸高效细胞工厂构建、合成生物学技术、基因编辑工具等领域取得了丰硕的成果。相关研究发表于Science Advances (2025,2020)、ACS Catalysis (2025,2018)、Nucleic Acids Research (2024,2022)、Nature Communications (2018)、Advanced Materials (2018)等本领域权威期刊。
